酵素を見る理由
なぜ酵素を見るのか?
私たちの体を構成している細胞が正常に働くことで、私たちは元気に生きられます。
細胞をうまく動かす道具が「タンパク質」です。タンパク質は色々な種類があり、その1つが「酵素」です。酵素にも色々な種類があり、ハサミの役割をする酵素や、ノリの役割をする酵素などがあります。
例えば、ハサミの役割をする酵素が通常よりも沢山のものを切ったり、逆に切らなくなると、細胞が正常に働かなくなります。この酵素の働きの異常が、病気の原因や悪化につながることが多く知られています。
私たちは、例えばハサミの役割をする酵素が「どれくらい切る力があるか?」を1分子のレベルで見ることができます。細胞の働きに直結した「酵素の働き」を見ることで、病気を正確に検出できるのです。
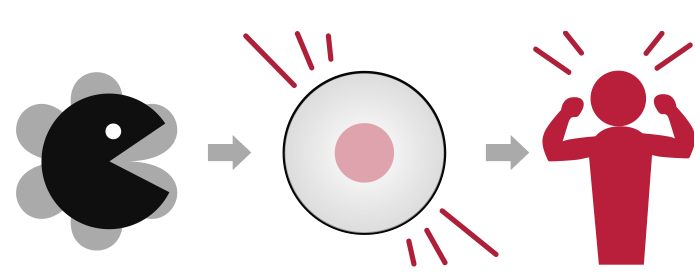
酵素が正常に働く場合
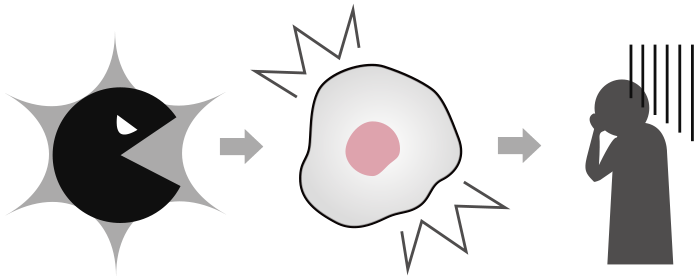
酵素が正常に働かない場合
遺伝子・RNA・タンパク質の検査と、何が違うの?
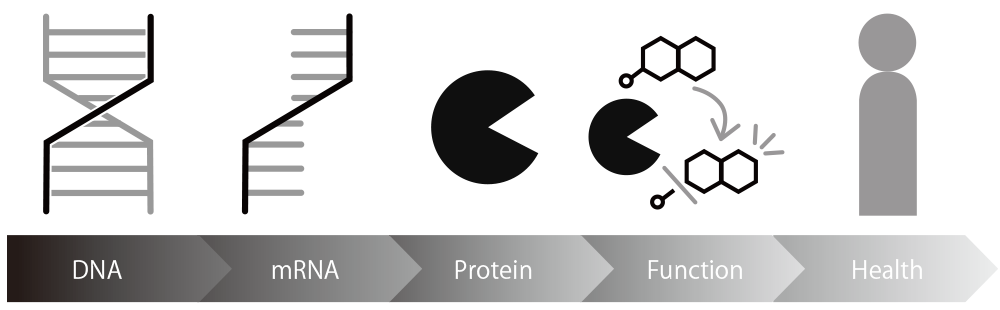
遺伝子は、タンパク質をつくるための設計図です。遺伝子の情報が読み取られてRNAという設計図に置き換えられ、その設計図をもとにタンパク質が作られます。そして、タンパク質が機能することによって細胞が働きます。
したがって、遺伝子、RNA、タンパク質の量は、細胞の働きや病気の状態にとって 「遠い情報」とも言えます。
一方、酵素を含むタンパク質が、たとえば "どれくらい切る力があるか" といった「性能」は、細胞の働きに「直結した情報」です。
私たちは酵素の量だけでなく、一つ一つの酵素の「性能」も見ることで、病気の状態を正確にとらえることができると考えています。
技術の詳細
東京大学の「酵素活性の蛍光検出」技術と、理化学研究所の「1分子計測」技術を組み合わせた、
独自の「1分子計測リキッドバイオプシー」で、血液中の様々な酵素の活性を1分子のレベルの超高感度で評価します。
1分子計測リキッドバイオプシー
STEP1 )
直径3μmのウェルを多数有するマイクロデバイスに、希釈血液と複数色の蛍光性酵素基質を加えます。確率論的に1個または0個の酵素が1ウェルの中に入ります。 酵素が蛍光性酵素基質を代謝すると蛍光物質がウェルに生じ、蛍光顕微鏡観察により酵素の活性に応じた強度の蛍光シグナルが得られます。
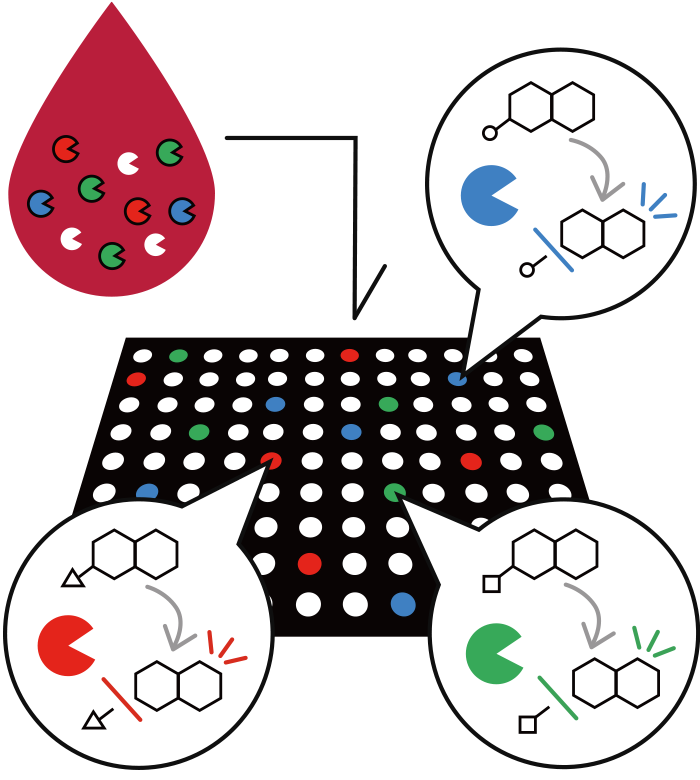
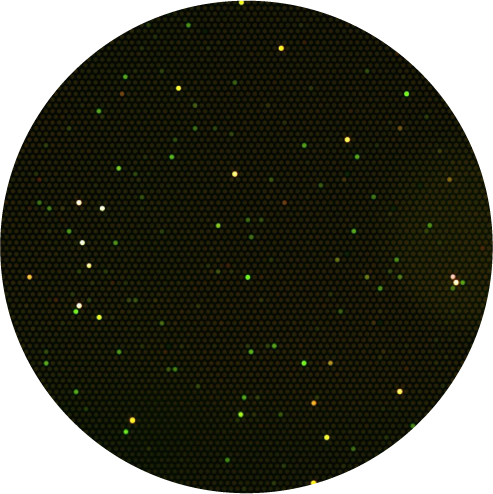
STEP2 )
光るウェルの数(酵素数)・各色の蛍光強度(酵素活性)の情報を持つ酵素活性プロファイルの相違に基づき、癌などの疾患を診断します。
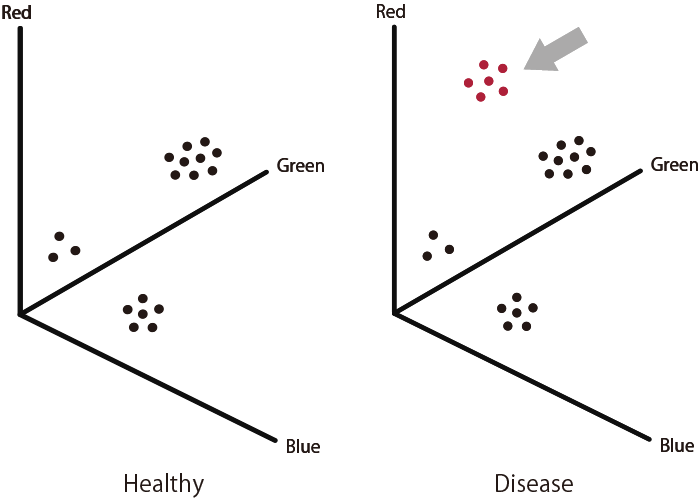
蛍光性酵素基質(蛍光プローブ)
「ある酵素(群)によって代謝されると光る」性質をもつ蛍光性酵素基質を、独自に設計・開発しています。
これまでに 100種以上の蛍光性酵素基質を開発しており、ALP (Alkaline phosphatases)・ENPP (Ectonucleotide pyrophosphatases/phosphodiesterases)・MMP (Matrix metalloproteinases)・DPP (Dipeptidyl peptidases)・Aminopeptidasesなど、様々な酵素の活性を網羅的に検出できています。
各色の蛍光性酵素基質に対する酵素の反応性の違いにより、酵素のサブタイプを見分けることも可能です。
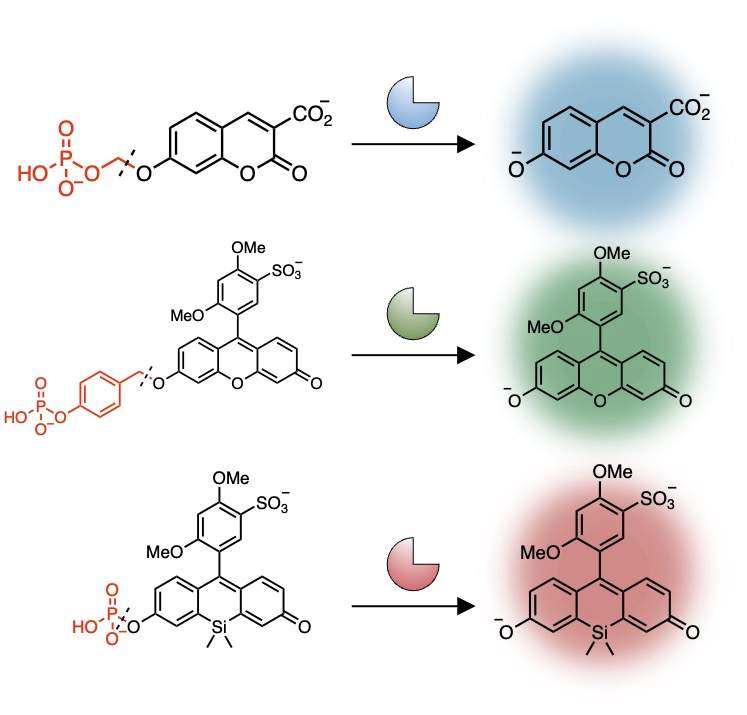
3つのメリット
高い予測精度
既存の診断・検査では、DNA、mRNA、酵素を含むタンパク質そのものを検出する技術が多く利用されていますが、これらの量の変化では疾患状態の変化を捉えられないことがあります。
私たちの技術は、細胞機能に直結し、より正確に疾患状態を反映すると考えられる「酵素の活性」(タンパク質の機能)を指標としています。
1分子ごとの酵素について活性の強さを捉えることで、予測精度の高い診断・検査が可能です。

高い検出感度
たとえば従来法であるELISA法では1000万個の酵素があって初めて検出可能となります。
私たちの技術ではマイクロデバイスを用いることで、酵素を1分子ずつ分けて検出でき、より早期の診断への応用が可能です。
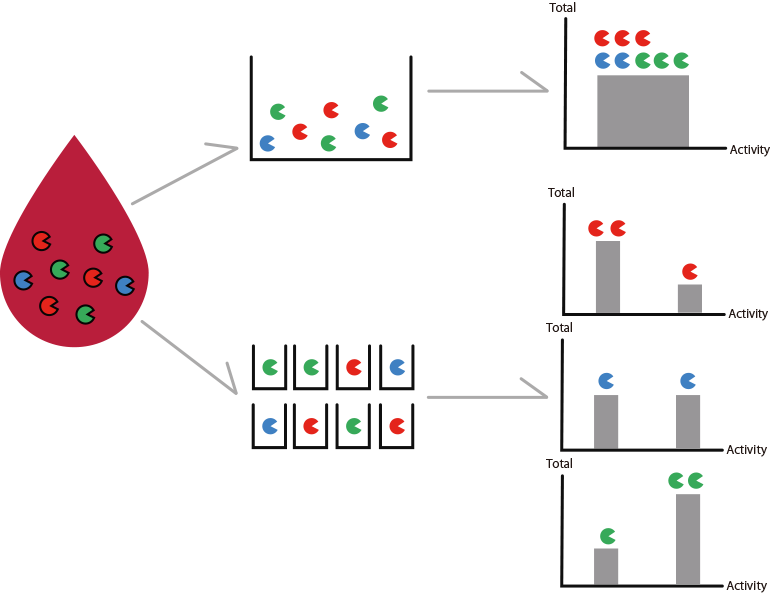
血液1滴以下で検出可能
1μLのほんのわずかな血液があれば十分に診断できるため、極少量の検体で評価が可能です。

研究実績
当社CTO坂本の大学院在籍時の研究成果。高水溶性の蛍光性酵素基質とマイクロデバイスを用いた1分子計測リキッドバイオプシー技術により、血液中の様々なリン酸エステル加水分解酵素の活性を単一分子レベルで且つサブタイプごとに検出できることを示した。さらに、すい臓癌患者の血液中では健常者と比較してENPP3の活性クラスターのサイズが有意に上昇していることを見出し、本技術の疾患診断への有用性を示した。
当社共同研究先の研究成果。M3 metallo protease活性を検出可能な新規蛍光性酵素基質を開発し、当該酵素の活性が大腸がん患者のがん組織及び血液で向上していることを見出し、1分子計測リキッドバイオプシー技術の大腸がん早期診断への応用性を示した。
当社の創業に向けたJST STARTでの研究成果。血液中の様々なタンパク質加水分解酵素の活性異常を1分子レベルで解析する方法を開発し、当該手法によりStage I-IIの膵臓がん患者の血液中でDPP4、CD13等の酵素の活性異常が生じていることを見出した。本知見に基づき1分子計測リキッドバイオプシー技術による膵臓がん早期診断の社会実装が進められている。
